Chemische energie gebruiken om elektriciteit te genereren
2024-07-15
5057
Catalogus

Figuur 1: Chemische energie
Geschiedenis van het chemische reactieproces
Het genereren van elektrische energie door chemische reacties begon in de 18e eeuw, een belangrijke mijlpaal in de wetenschappelijke geschiedenis.Luigi Galvani's baanbrekende onderzoek, gepubliceerd in 1792, leidde tot een dieper begrip van bio -elektrische fenomenen.De experimenten van Galvani met kikkerbenen onthulden dat dierlijke weefsels elektrische stromen konden produceren, die hij 'dierlijke elektriciteit' noemde.Voortbouwend op de bevindingen van Galvani, ontwikkelde Alessandro Volta de Voltaic -stapel in 1800, de eerste echte batterij.De voltaische stapel gebruikte afwisselende schijven van zilver en zink, gescheiden door poreuze materialen gedrenkt in een zoutwateroplossing, waardoor een gestage elektrische stroom ontstaat.Volta's grondige documentatie van zijn experimenten en resultaten gepresenteerd aan de Royal Society of London, stimuleerde uitgebreid onderzoek naar de aard en potentiële toepassingen van elektriciteit.
Definitie van chemische energie
Chemische energie is een van de zes primaire vormen van energie: elektrisch, stralend, mechanisch, thermisch en nucleair.Hoewel er andere vormen zijn, zoals elektrochemisch, geluid en elektromagnetisch, combineert chemische energie deze zes voornamelijk.Deze onderlinge verbindingen stellen energieopwekking op verschillende manieren mogelijk.Ideaal om werk te doen, wat in wetenschappelijke termen betekent dat ze kracht toepassen om een object over een afstand te verplaatsen.Chemische energie brengt energie vrij wanneer chemische potentiële energie reageert.Op moleculair niveau woont chemische energie in de bindingen van chemische verbindingen.Tijdens een reactie interageren deze moleculen, die mogelijk nieuwe stoffen vormen en energie vrijgeven, die vervolgens kunnen worden vastgelegd en gebruikt voor werk.Koken water absorbeert bijvoorbeeld warmte in een endotherme reactie, waardoor vloeistof in damp verandert.Omgekeerd, wanneer stoom terug in vloeistof condenseert, laat het warmte vrij in een exotherme reactie.Deze continue cyclus van absorptie en afgifte toont de belangrijkste rol van chemische energie in verschillende processen, van het alledaagse tot het buitengewone.
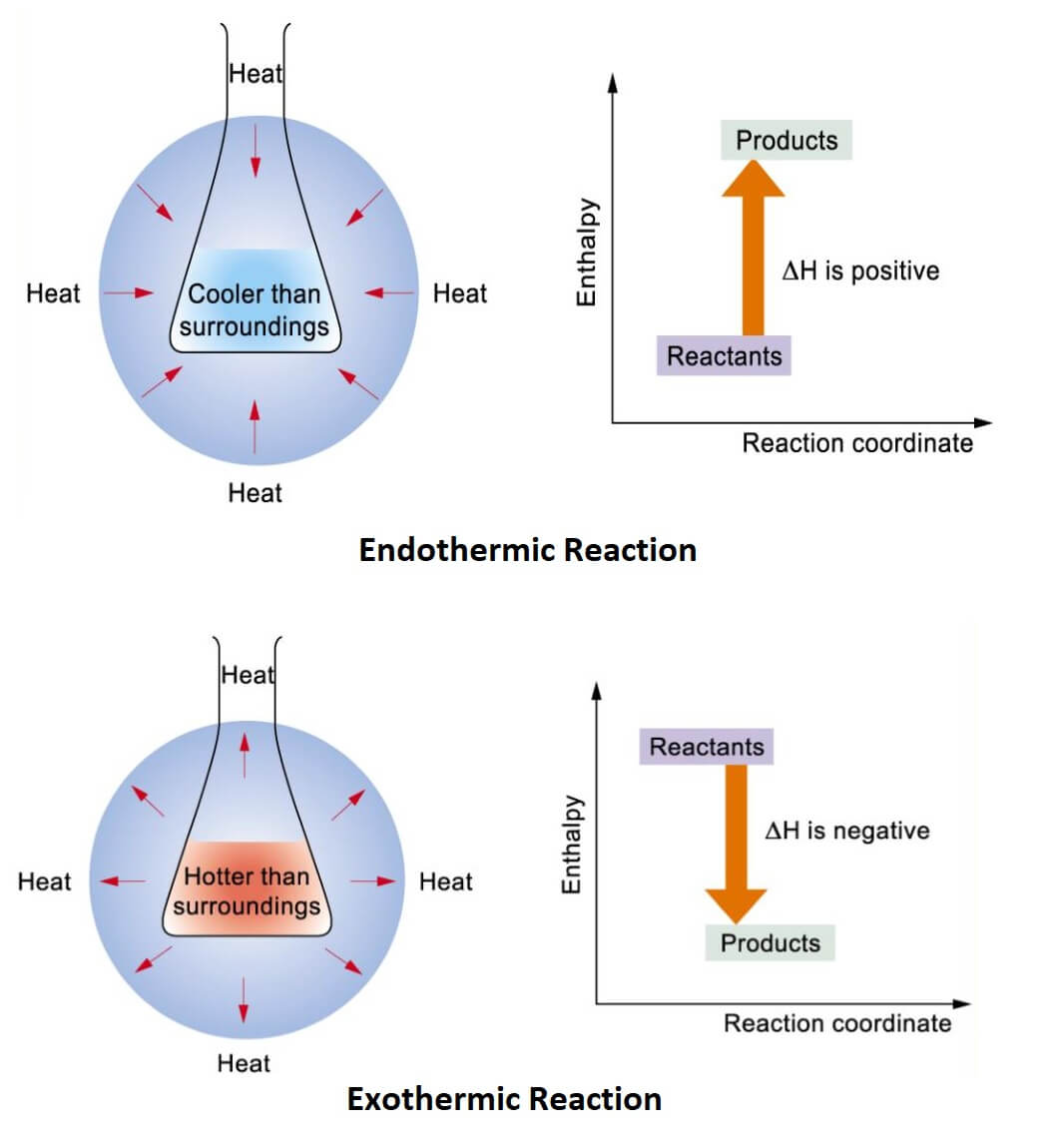
Figuur 2: Endotherme reactie versus exotherme reactie
Bij het raken van een match genereert de wrijving voldoende warmte om een chemische reactie te starten in de verbindingen van de wedstrijdkop.Deze reactie geeft energie vrij als warmte en licht, en toont de omzetting van chemische energie in bruikbaar werk.In ons lichaam omzet chemische energie uit voedsel in kinetische energie voor beweging en thermische energie voor lichaamstemperatuuronderhoud.Batterijen slaan chemische energie op die omzet in elektrische energie om apparaten te voeden.Een smartphone -batterij bevat bijvoorbeeld chemische verbindingen die een gecontroleerde reactie ondergaan wanneer ze worden gebruikt, waardoor energie wordt vrijgegeven die het apparaat aandrijft.Dit proces omvat microscopische bewerkingen om een consistente en betrouwbare energievoorziening te garanderen.Het gebruik van chemische energie omvat het begrijpen en beheren van deze reacties om de efficiëntie en veiligheid te optimaliseren.In industriële toepassingen is de precieze controle van de temperatuur- en drukomstandigheden vereist om de energieproductie te maximaliseren en tegelijkertijd de risico's te minimaliseren.In wetenschappelijk onderzoek kan experimenteren met verschillende chemische verbindingen efficiëntere oplossingen voor energieopslag ontwikkelen, zoals geavanceerde batterijen met hogere capaciteiten en snellere laadtijden.Een gedetailleerd begrip en manipulatie van chemische energieprocessen zijn vereist voor veel technologische vooruitgang en dagelijkse toepassingen, die de diepgaande impact van deze energievorm op onze wereld presenteren.
Elektriciteit genereren door chemische reacties
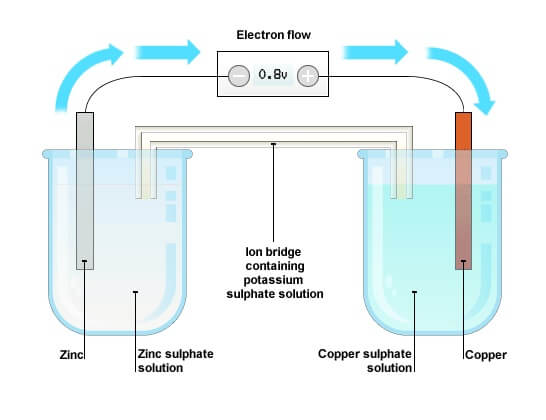
Figuur 3: De procedure van chemische reacties produceert elektriciteit
De voltaische stapel - met zijn afwisselende zilver- en zinkschijven gescheiden door poreus materiaal gedrenkt in zout water, illustreert de belangrijkste principes van het genereren van elektriciteit door chemische reacties.De zilveren terminal werkt als de positieve elektrode, terwijl de zinkterminal dient als de negatieve elektrode.Volta's verbeteringen in het gebruik van koper- en zinkplaten in een loogoplossing, toonden aan hoe verschillende materialen de efficiëntie kunnen stimuleren.Een chemische cel, de kerneenheid van de elektriciteitsproductie, werkt door een bijna constante spanning te handhaven door twee metalen elektroden die zijn ondergedompeld in een zure of alkalische oplossing.Een typische chemische cel kan koper- en zinkelektroden gebruiken in een loogoplossing.Meerdere cellen vormen een batterij, die dient als een directe stroom (DC) spanningsbron, die chemische energie omzet in elektrische energie.De configuratie - serie of parallel - geeft de totale spanning en stroomuitgang vast.In serie tellen individuele celspanningen op, terwijl ze parallel worden gecombineerd, die een consistente spanning behouden.
De werking van een chemische cel begint met onderdompelende elektroden van verschillende metalen in een elektrolyt (die een zuur-, alkalische of zoutoplossing kan zijn.) De elektrolyt is ideaal voor het ionisatieproces, waarbij atomen en moleculen worden gesplitst in elektrisch geladen deeltjes die ionen worden genoemd,het vaststellen van een ionische balans in de oplossing.Wanneer een zinkelektrode wordt ondergedompeld in de elektrolyt, lost deze gedeeltelijk op, waardoor positief geladen zinkionen produceert en vrije elektronen op de elektrode achterlaat - waardoor een negatieve lading ontstaat.Een koperelektrode in dezelfde oplossing trekt positieve waterstofionen aan, neutraliseert ze en vormt waterstofgasbellen.Deze interactie genereert een elektrische potentiaal tussen de elektroden.De omvang van het potentieel, ongeveer 1,08 volt voor een zink-koper-cel, hangt af van de gebruikte metalen.Dit potentieel wordt gehandhaafd door voortdurende chemische reacties totdat een belasting is verbonden, waardoor elektronen van de negatieve zinkelektrode naar de positieve koperelektrode kunnen stromen.Ten slotte, het genereren van een elektrische stroom.
Het construeren en bedienen van een dergelijke chemische cel vereist zorgvuldige aandacht voor detail.De operator moet ervoor zorgen dat de zuiverheid en de juiste afmetingen van de metaalschijven de elektrolytoplossing nauwkeurig voorbereiden en de componenten zorgvuldig assembleren.Dit is om kort circuits te voorkomen en de efficiëntie te maximaliseren.Bij het monteren van een voltaische stapel moet het poreuze materiaal bijvoorbeeld grondig worden geweekt in zoutwater om de consistente geleidbaarheid tussen de schijven te behouden.Zorgen voor een veilige verbinding van de geleiders aan elk uiteinde is vereist voor stabiele elektrische uitgang.Deze principes strekken zich uit tot verschillende moderne apparaten en systemen.Het assembleren van batterijen voor elektronische apparaten vereist bijvoorbeeld dat technici de cellen nauwgezet afstemmen, de optimale elektrolytconcentratie behouden en alle verbindingen voor betrouwbare prestaties beveiligen.In industriële omgevingen is precieze controle over temperatuur- en drukomstandigheden tijdens de werking van chemische cellen ideaal voor het maximaliseren van de energie -output en het waarborgen van de veiligheid.Het begrijpen en beheren van deze subtiele operationele details verbeteren de efficiëntie en betrouwbaarheid van chemische energieconversieprocessen - en benadrukt hun rol bij het aandrijven van een breed scala aan technologieën.
Chemische energie -conversie in dagelijkse elektronica
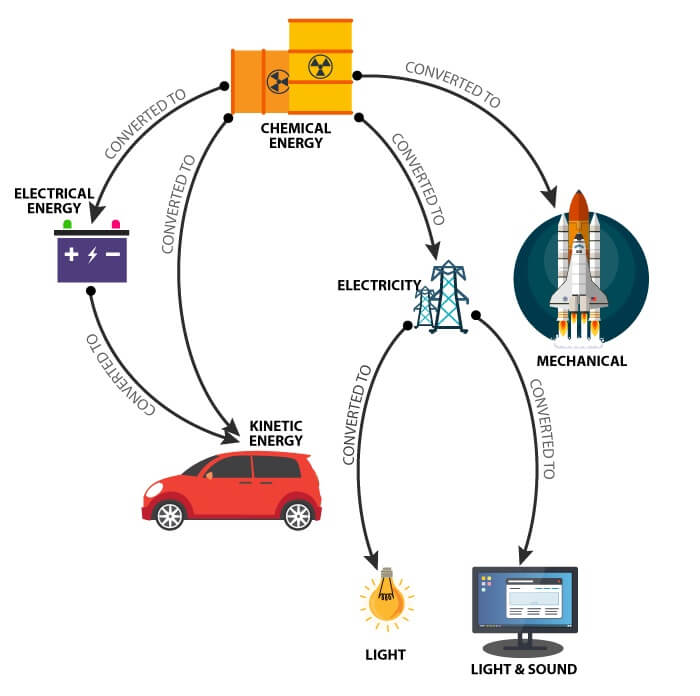
Figuur 4: Chemische energie omgezet in alledaagse elektronica
Het omzetten van chemische energie in elektrische energie via cellen en batterijen is ideaal voor moderne elektronica.Deze technologie, prominent sinds telegraafsystemen in de jaren 1830, verhoogde de commerciële batterijproductie en transformeerde deze in een lucratieve industrie.Tegen de jaren 1870 zagen batterijen elektrische klokken, en tegen 1900 zagen de productie van de zaklamp meer dan twee miljoen batterijen.Deze technologische progressie is doorgegaan, waarbij batterijen centraal staan in vele hedendaagse toepassingen.Tegenwoordig worden batterijen gebruikt in veel apparaten en systemen.Batterijbewerking omvat ingewikkelde stappen, die elk precisie en begrip vereisen.Bij het starten van een interne verbrandingsmotor levert de batterij van het voertuig de elektrische energie om de startmotor van stroom te voorzien en de motor te ontsteken.Dit vereist dat de batterij een stabiele lading handhaaft, bereikt door goed onderhoud, zoals regelmatige controles op elektrolytniveaus en reinigen - Beveilig terminalverbindingen om corrosie te voorkomen en een efficiënte stroomoverdracht te garanderen.
Batterij-aangedreven vorkheftrucks worden veel gebruikt waar de uitlaat van de benzinemotor uitlaatrisico's voor gezondheidsrisico's opleveren.Deze batterijen moeten routinematig worden opgeladen en geïnspecteerd op slijtage of schade.Technici volgen een gedetailleerd protocol: het controleren van spanningsniveaus, het inspecteren van de elektrolytconcentratie en ervoor zorgen dat de laadapparatuur correct werkt.Deze zorgvuldige aandacht zorgt ervoor dat de vorkheftrucks betrouwbaar en veilig blijven.Het ontwikkelen van efficiëntere batterijen voor elektrische voertuigen (EV's) is een substantieel onderzoeksgebied.Deze batterijen hebben geavanceerde materialen en precieze productie nodig om hogere energiedichtheden en langere levensduur te bereiken.Onderzoekers en ingenieurs werken aan het verbeteren van de kathode- en anodematerialen - het optimaliseren van de elektrolytensamenstelling en het verbeteren van het thermische beheer om oververhitting te voorkomen, plus de levensduur van de batterij verlengen.Draagbare audio -apparaten, zoals CD -spelers, en moderne elektronica zoals smartphones en laptops, zijn sterk afhankelijk van batterijen.Het gebruik van deze apparaten omvat het begrijpen van batterijbeheerprincipes om de levensduur en prestaties te maximaliseren.Gebruikers moeten bijvoorbeeld diepe lozingen vermijden en de juiste oplaadcycli volgen om de gezondheid van de batterij te behouden.Fabrikanten gebruiken Battery Management Systems (BMS) om de toestand van lading, temperatuur en algehele batterijgezondheid te controleren en te beheren.
Evenzo zijn de batterijen vereist functies in polshorloges en desktopcomputers - het handhaven van tijd- en geheugenfuncties, zelfs wanneer het hoofdvermogen is uitgeschakeld.In polshorloges moet de batterij compact maar krachtig genoeg zijn om jaren mee te gaan.Het assemblageproces omvat het plaatsen van de kleine batterij in zijn compartiment met precisiegereedschap, waardoor een goed contact met het interne circuit wordt gewaarborgd zonder schade te veroorzaken.Laptops kunnen volledig werken op batterijvermogen, wat de belangrijkste rol van chemische energie -conversie bij het bieden van mobiliteit benadrukt.Het samenstellen van laptopbatterijen omvat het regelen van cellen in een compacte en efficiënte configuratie.Deze batterijen worden vaak gevolgd door een BMS om laad- en ontladingscycli in evenwicht te brengen om overladen te voorkomen en de levensduur van de batterij te verlengen.Gebruikers moeten specifieke laadpraktijken volgen, zoals het vermijden van volledige lozingen en het niet continu aangesloten laptop om de batterijefficiëntie te behouden.De evolutie en toepassing van batterijen benadrukken de transformerende impact van chemische energieconversie op de dagelijkse elektronica.Van vroege telegraafsystemen tot de geavanceerde apparaten van vandaag, het opslaan en vrijgeven van elektrische energie door chemische reacties stimuleert innovatie en verbetert de functionaliteit van talloze technologieën.
Milieueffecten van het gebruik van chemische energie voor elektriciteit
Het gebruik van chemische energie voor het genereren van elektriciteit, voornamelijk door batterijen en brandstofcellen, heeft aanzienlijke omgevingseffecten, zowel positief als negatief.Het begrijpen van deze effecten is vereist voor het nemen van geïnformeerde beslissingen over energieproductie en -gebruik.
Positieve gevolgen voor het milieu.Een van de belangrijkste voordelen van het gebruik van chemische energie (vooral in de vorm van batterijen) is de vermindering van de uitstoot van broeikasgassen in vergelijking met traditionele fossiele brandstoffen.Elektrische voertuigen (EV's) aangedreven door lithium-ionbatterijen produceren nul-uitlaatemissies, opmerkelijk verminderen van luchtvervuiling en bijdragen aan schonere stedelijke omgevingen.Evenzo kunnen opslagsystemen voor hernieuwbare energie met chemische batterijen elektriciteit opslaan en verzenden die wordt gegenereerd uit hernieuwbare bronnen zoals zonne- en wind.Een meer consistente en betrouwbare levering van hernieuwbare energieverlening mogelijk maken.
Negatieve milieueffecten.Ondanks deze voordelen zijn er verschillende milieuproblemen in verband met de productie, het gebruik en de verwijdering van chemische batterijen.De extractie van grondstoffen zoals lithium, kobalt en nikkel, ideaal voor de productie van batterijen, kan leiden tot grote aantasting van het milieu.Mijnbouwactiviteiten leiden vaak tot habitatvernietiging, watervervuiling en verhoogde koolstofemissies.Bovendien zijn deze materialen eindig en is hun extractie niet altijd duurzaam.Het productieproces van batterijen zelf is ook energie-intensief en kan aanzienlijke emissies en afval veroorzaken.Fabrieken die batterijen produceren, verbruiken grote hoeveelheden energie, vaak afgeleid van niet-hernieuwbare bronnen, wat leidt tot een hogere CO2-voetafdruk.Wat meer is, het productieproces omvat gevaarlijke chemicaliën, zo niet goed beheerd, kan leiden tot milieuvervuiling.
Verwijderings- en recycling -uitdagingen.De verwijdering van batterijen aan het einde van de levensduur vormt een andere belangrijke milieu-uitdaging.Batterijen bevatten giftige stoffen zoals lood, cadmium en zuren.Deze kunnen in bodem en water uitlogen als ze niet goed worden verwijderd.Onjuiste verwijdering van batterijen in stortplaatsen kan leiden tot milieuverontreiniging en risico's vormen voor de menselijke gezondheid.Recyclingbatterijen is een enorme stap in het verminderen van deze negatieve effecten.Het recyclingproces is echter complex en niet universeel geïmplementeerd.Hoewel recycling waardevolle materialen kan herstellen en de behoefte aan nieuwe extractie van grondstof kan verminderen, is het vaak duur plus technisch uitdagend.Veel regio's missen voldoende recyclinginfrastructuur, wat leidt tot lage recyclingpercentages en voortdurende schade aan het milieu door onjuiste batterijverwijdering.
Het verzachten van milieueffecten.Er worden inspanningen geleverd om de milieueffecten van het gebruik van chemische energie voor elektriciteit te verminderen.Innovaties in batterijtechnologie zijn gericht op het verminderen van de afhankelijkheid van zeldzame en toxische materialen, het verhogen van de energiedichtheid en het verbeteren van de recyclebaarheid.Onderzoekers onderzoeken bijvoorbeeld alternatieven zoals batterijen van vaste toestand en lithium-zwavelbatterijen, die een hogere efficiëntie en lagere milieu-impact beloven.Overheden en marktleiders werken aan het ontwikkelen van efficiëntere recyclingmethoden en het implementeren van voorschriften die de juiste verwijdering en recycling van batterijen aanmoedigen.Publieke bewustmakingscampagnes kunnen ook een rol spelen bij het opleiden van consumenten over het belang van batterijrecycling.
Conclusie
Concluderend heeft chemische energie -conversie het technologische landschap opmerkelijk gevormd - van zijn vroege dagen met Galvani en Volta tot zijn moderne toepassingen in de dagelijkse elektronica.Door de principes van chemische reacties te beheersen en de ingewikkelde betrokken processen nauwgezet te beheren, hebben we betrouwbare oplossingen voor energieopslag zoals batterijen ontwikkeld die een breed scala aan apparaten voeden.Deze reis onderstreept de transformerende kracht van chemische energie bij het stimuleren van innovatie, het verbeteren van de functionaliteit en het voldoen aan de energievereisten van de hedendaagse samenleving.Terwijl onderzoek de grenzen van efficiëntie en capaciteit blijft verleggen, belooft de toekomst van chemische energieconversie nog grotere vooruitgang.Wees gerust dat deze energievorm opmerkelijk blijft voor technologische vooruitgang en het dagelijkse leven.
Veelgestelde vragen [FAQ]
1. Hoe zetten batterijen chemische energie om in elektrische energie?
Batterijen zetten chemische energie om in elektrische energie door elektrochemische reacties.In een batterij zijn er twee elektroden: een anode en een kathode, gescheiden door een elektrolyt.Wanneer de batterij is aangesloten op een apparaat, treedt een chemische reactie op tussen de anode en de elektrolyt, waardoor elektronen worden vrijgelaten.Deze elektronen stromen door een extern circuit naar de kathode en genereren een elektrische stroom die het apparaat aandrijft.De elektrolyt vergemakkelijkt de beweging van ionen in de batterij om de stroom van elektronen in evenwicht te brengen.Dit proces gaat door totdat de reactanten zijn uitgeput, op welk punt de batterij moet worden opgeladen of vervangen.
2. Hoe efficiënt is het proces van het omzetten van chemische energie naar elektrische energie?
De efficiëntie van het omzetten van chemische energie in elektrische energie in batterijen varieert maar varieert meestal van 70% tot 90%.Dit betekent dat 70% tot 90% van de chemische energie wordt omgezet in elektrische energie, terwijl de rest verloren gaat als warmte.Factoren die de efficiëntie beïnvloeden, zijn onder meer het type batterij, de gebruikte materialen en de bedrijfsomstandigheden.Lithium-ionbatterijen staan bijvoorbeeld bekend om hun hoge efficiëntie en worden veel gebruikt in consumentenelektronica en elektrische voertuigen.Alle batterijen ervaren echter enig energieverlies als gevolg van interne weerstand en andere factoren, wat hun algehele efficiëntie enigszins vermindert.
3. Wat is het verschil tussen chemische energie in batterijen en brandstofcellen?
Zowel batterijen als brandstofcellen zetten chemische energie om in elektrische energie, maar ze werken anders.Batterijen slaan chemische energie op in hun cellen en ontladen deze door interne reacties.Het zijn zelfstandige systemen die meerdere keren kunnen worden opgeladen en hergebruikt.Brandstofcellen daarentegen omzetten continu chemische energie om van een externe brandstofbron (zoals waterstof) in elektriciteit.Ze vereisen een constante toevoer van brandstof en zuurstof om stroom te blijven genereren.Hoewel batterijen geschikt zijn voor draagbare en kleinere toepassingen, worden brandstofcellen vaak gebruikt voor grotere en continue stroombehoeften, zoals in voertuigen en stationaire stroomopwekking.
4. Wat zijn de beperkingen van het gebruik van chemische energie als een bron van elektrische energie?
Het gebruik van chemische energie als een bron van elektrische energie heeft verschillende beperkingen.Ten eerste is de capaciteit van batterijen eindig, wat betekent dat ze moeten worden opgeladen of vervangen zodra ze zijn uitgeput.Dit kan onhandig zijn voor toepassingen die langdurig vermogen vereisen.Ten tweede kan de productie en verwijdering van batterijen milieu -uitdagingen opleveren vanwege het gebruik van giftige materialen en potentieel voor vervuiling.Bovendien hebben batterijen een beperkte levensduur, waarbij vaak vervanging nodig is na een bepaald aantal ladingscycli.Temperatuurgevoeligheid is een ander probleem;Extreme temperaturen kunnen de batterijprestaties en de levensduur beïnvloeden.Ten slotte, terwijl er vooruitgang wordt geboekt, blijven energiedichtheid en opslagmogelijkheden van batterijen nog steeds achter bij andere vormen van energieopslag, zoals fossiele brandstoffen.
5. Hoe lang kunnen apparaten door chemische energie duren voordat ze een opladen of vervanging nodig hebben?
De duur die apparaten aangedreven door chemische energie kunnen duren voordat ze een opladen of vervanging nodig hebben, hangt af van verschillende factoren, waaronder het type batterij, het energieverbruik van het apparaat en de capaciteit van de batterij.Een smartphone met een lithium-ionbatterij kan bijvoorbeeld een volledige dag duren op een enkele lading met typisch gebruik, terwijl een smartwatch mogelijk enkele dagen duurt.Grotere apparaten, zoals elektrische voertuigen, kunnen honderden kilometers op een enkele lading reizen.Naarmate de batterijen verouderen, neemt hun capaciteit echter af, waardoor de tijd tussen ladingen wordt verkort.Oplaadbare batterijen hebben meestal een levensduur van enkele honderden tot een paar duizend ladingscycli voordat hun prestaties aanzienlijk afnemen, waardoor vervanging nodig is.
 OVER ONS
Klanttevredenheid elke keer.Wederzijds vertrouwen en gemeenschappelijke belangen.
OVER ONS
Klanttevredenheid elke keer.Wederzijds vertrouwen en gemeenschappelijke belangen.
Functietest.De hoogste kosteneffectieve producten en de beste service zijn onze eeuwige inzet.
Heet artikel
- Zijn CR2032 en CR2016 uitwisselbaar
- MOSFET: Definitie, werkingsprincipe en selectie
- Relaisinstallatie en testen, interpretatie van relaisbedradingsdiagrammen
- CR2016 vs. CR2032 Wat is het verschil
- NPN vs. PNP: Wat is het verschil?
- ESP32 vs STM32: Welke microcontroller is beter voor u?
- LM358 Dubbele operationele versterker uitgebreide gids: pinouts, circuitdiagrammen, equivalenten, nuttige voorbeelden
- CR2032 vs DL2032 vs CR2025 Vergelijkingsgids
- Inzicht in de verschillen ESP32 en ESP32-S3 Technische en prestatie-analyse
- Gedetailleerde analyse van RC Series Circuit
 Navigeren door de selectie van spanningsregelaars: een uitgebreide gids
Navigeren door de selectie van spanningsregelaars: een uitgebreide gids
2024-07-15
 L293D vs L298N: Het verschil tussen L293D en L298N
L293D vs L298N: Het verschil tussen L293D en L298N
2024-07-12
Heet onderdeelnummer
 CKG57NX7S2A226M500JJ
CKG57NX7S2A226M500JJ SMK325B7333KNHT
SMK325B7333KNHT GRM1555C2A5R8CA01J
GRM1555C2A5R8CA01J GJM0335C1E330JB01D
GJM0335C1E330JB01D GRM1887U1H103JA01J
GRM1887U1H103JA01J 08052U1R7BAT2A
08052U1R7BAT2A DX-5R5H334U
DX-5R5H334U ZHR-5
ZHR-5 9FG830AGLF
9FG830AGLF ATF1504AS-10JU44
ATF1504AS-10JU44
- RT0402BRD07750RL
- GAL16V8D-15LPN
- MC908EY16ACFJER
- AT29BV020-15JU
- XRT7296IWTR-F
- CM150DC1-24NFM
- AD5522JSVUZ
- PCM3000E
- SN761663DGKRG4
- FDC5612
- MSP430F5510IRGCT
- TLC7528IDWR
- ADT75ARZ-REEL
- TMP275AIDGKR
- ADS8323YB/250
- T491D227M010AT4053
- T491A335M006AT
- T378E226K015AS
- 78M12
- ADV7171KS
- EPH1100KSHSQ
- FDC37C672
- HC55185GCM
- IS61LV256-8J
- LA5317M-S-TP-T1
- LFEC3E-5TN144C-4I
- MN101C30ABP
- PALCE26V12H-15JC
- PC87366-ICK/VLA
- SP3226EEA
- A2S28D40CTP-G5PP
- CM7R-022
- S10313V1
- TMS44400-60DJ
- ADC0838ACN
- S5L931CX01
- ZIVA-HGI-BA4
- ML66Q592-867TCZ200
- TPCP8507